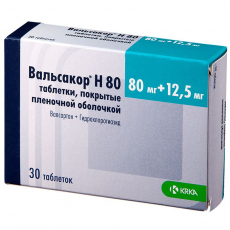
Вальсакор HД 160 таб ппо 160мг+25мг №30

В наличии в 35 аптеках . Бронь препарата в течение 3 дней - Бесплатно
Оплата при получении наличными или банковской картой
Цена действительна только для интернет заказов, итоговую стоимость препаратов уточняйте на кассе в аптеке
Внешний вид товара может отличаться от изображенного на фотографии
Отметьте любимую аптеку и вы всегда будете видеть её первой в списке
В наличии больше 3 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
8:00 — 22:00
798.00Р
В наличии меньше 3 шт.
8:00 — 20:00
798.00Р
Осталась 1 шт.
8:00 — 20:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
В наличии меньше 3 шт.
8:00 — 20:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
В наличии меньше 3 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
8:00 — 20:00
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
В наличии меньше 3 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
8:00 — 22:00
798.00Р
В наличии меньше 3 шт.
8:00 — 20:00
798.00Р
Осталась 1 шт.
8.00 - 20.00
798.00Р
В наличии меньше 3 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
8:00 — 22:00
798.00Р
Осталась 1 шт.
Круглосуточно
798.00Р
Осталась 1 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
8:00 — 21:00
798.00Р
Осталась 1 шт.
9:00 — 22:00
798.00Р
В наличии меньше 3 шт.
8:00 — 21:00
798.00Р
В наличии меньше 3 шт.
8:00 — 20:00
798.00Р
В наличии меньше 3 шт.
8:00 — 20:00
798.00Р
Определить моё местоположение
Код АТХ
C09DA03
МНН / Группировочное наименование / Химическое наименование
валсартан + гидрохлоротиазид
Фармако-терапевтическая группа
гипотензивное средство комбинированное (ангиотензина II рецепторов антагонист + диуретик)
Передозировка
Симптомы: основным ожидаемым проявлением передозировки валсартана является выраженное снижение АД, которое может привести к нарушению сознания, коллапсу и/или шоку. При передозировке гидрохлоротиазида возможно развитие следующих симптомов: тошнота, сонливость, снижение ОЦК, нарушения ритма сердца и спазм мышц, вызванные нарушением водно-электролитного баланса.
Лечение: симптоматическое и зависит от времени, прошедшего с момента приема препарата, и от степени тяжести симптомов. В случае ранней диагностики передозировки рекомендовано вызвать рвоту и/или промыть желудок. Следует стабилизировать показатели гемодинамики. При выраженном снижении АД необходимо перевести пациента в горизонтальное положение с приподнятыми вверх ногами и восполнить ОЦК (в/в ввести 0,9 % раствор натрия хлорида) под контролем показателей гемодинамики и диуреза. Валсартан не выводится с помощью гемодиализа, так как значительная его часть связывается с белками плазмы крови. Гидрохлоротиазид выводится с помощью гемодиализа.
Применение детьми
Противопоказан лицам в возрасте до 18 лет (эффективность и безопасность применения у детей не доказаны).
Условия отпуска
Отпускают по рецепту.
Срок годности
5 лет.
Не применять препарат по истечении срока годности.
Применение при хронических заболеваниях
Пациенты пожилого возраста (старше 65 лет)
AUC валсартана у некоторых пациентов пожилого возраста больше, чем у добровольцев молодого возраста. Данные изменения клинического значения не имеют.
Предположительно, у пациентов пожилого возраста с нормальным уровнем АД и артериальной гипертензией системный клиренс гидрохлоротиазида ниже, чем у здоровых молодых добровольцев.
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек с клиренсом креатинина (КК) 30-70 мл/мин коррекции дозы препарата Вальсакор® НД 160 не требуется. Нет данных по применению препарата у пациентов с нарушением функции почек тяжелой степени (КК менее 30 мл/мин) и у пациентов, находящихся на гемодиализе. Валсартан не выводится с помощью гемодиализа, в отличие от гидрохлоротиазида.
При наличии почечной недостаточности Cmax и AUC гидрохлоротиазида увеличиваются, а скорость выведения снижается. У пациентов с нарушением функции почек легкой и средней степени тяжести T½ гидрохлоротиазида удлиняется практически в два раза.
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени легкой (5-6 баллов по шкале Чайлд-Пью) или средней (7-9 баллов по шкале Чайлд-Пью) степени тяжести AUC валсартана в два раза больше, чем у здоровых добровольцев. Нет данных по применению валсартана у пациентов с нарушением функции печени тяжелой степени (более 9 баллов по шкале Чайлд-Пью).
Заболевания печени не оказывают существенного влияния на фармакокинетику гидрохлоротиазида, поэтому коррекции его дозы в данном случае не требуется.
У пациентов с обструкцией желчевыводящих путей препарат Вальсакор® НД 160 следует применять с осторожностью.
Состав
1 таблетка, покрытая пленочной оболочкой, содержит:
Ядро:
Действующие вещества: валсартан 160,00 мг, гидрохлоротиазид 25,00 мг
Вспомогательные вещества: целлюлоза микрокристаллическая, кроскармеллоза натрия, повидон-K25, лактозы моногидрат, магния стеарат, кремния диоксид коллоидный
Оболочка пленочная: гипромеллоза 2910, титана диоксид (Е171), макрогол-4000, краситель железа оксид красный (Е172), краситель железа оксид желтый (Е172)
Описание
Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой светло-коричневого цвета.
Вид на изломе: белая шероховатая масса с пленочной оболочкой светло-коричневого цвета.
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 160 мг + 25 мг.
При производстве на АО «КРКА, д.д., Ново место», Словения:
По 7, 10, 14 или 15 таблеток в блистере (контурной ячейковой упаковке) из комбинированного материала ПВХ/ПЭ/ПВДХ и алюминиевой фольги.
По 4, 8, 12 или 14 блистеров (контурных ячейковых упаковок) по 7 таблеток, или по 3, 6 или 9 блистеров (контурных ячейковых упаковок) по 10 таблеток, или по 2, 4, 6 или 7 блистеров (контурных ячейковых упаковок) по 14 таблеток, или по 2, 4 или 6 блистеров (контурных ячейковых упаковок) по 15 таблеток помещают в пачку картонную вместе с инструкцией по применению.
При производстве на ООО «КРКА-РУС», Россия:
По 7, 10, 14 или 15 таблеток в контурной ячейковой упаковке (блистере) из комбинированного материала ПВХ/ПЭ/ПВДХ и алюминиевой фольги.
По 4, 8, 12 или 14 контурных ячейковых упаковок (блистеров) по 7 таблеток, или по 3, 6 или 9 контурных ячейковых упаковок (блистеров) по 10 таблеток, или по 2, 4, 6 или 7 контурных ячейковых упаковок (блистеров) по 14 таблеток, или по 2, 4 или 6 контурных ячейковых упаковок (блистеров) по 15 таблеток помещают в пачку из картона вместе с инструкцией по применению.
Показания к применению
Артериальная гипертензия (пациентам, которым показана комбинированная терапия).
Побочное действие
Классификация частоты развития побочных эффектов, рекомендованная Всемирной организацией здравоохранения (ВОЗ): очень часто (≥ 1/10), часто (от ≥ 1/100 до < 1/10), нечасто (от ≥ 1/1000 до < 1/10), редко (от ≥ 1/10000 до < 1/1000), очень редко (< 1/10000), частота неизвестна (не может быть оценена на основе имеющихся данных).
|
Системно-органный класс |
Нежелательная реакция (НР) |
Валсартан + гидрохлоро-тиазид |
Валсартан |
Гидрохлоро-тиазид |
|
Нарушения со стороны крови и лимфатической системы |
Снижение гемоглобина Cнижение гематокрита Тромбоцитопения |
- |
Частота неизвестна |
- |
|
Тромбоцитопения, ингода с пурпурой |
- |
- |
Редко |
|
|
Агранулоцитоз Угнетение костномозгового кроветворения Гемолитическая анемия Лейкопения |
- |
- |
Очень редко |
|
|
Апластическая анемия |
- |
- |
Частота неизвестна |
|
|
Нарушения со стороны иммунной системы |
Реакции гиперчувствитель-ности |
- |
Частота неизвестна |
Очень редко |
|
Аллергические реакции, включая сывороточную болезнь |
- |
Частота неизвестна |
- |
|
|
Нарушения со стороны обмена веществ и питания |
Дегидратация |
Нечасто |
- |
|
|
Повышение содержания калия в сыворотке крови |
- |
Частота неизвестна |
- |
|
|
Гипонатриемия |
- |
Частота неизвестна |
Часто |
|
|
Гипокалиемия Повышение концентрации липидов в плазме крови |
- |
- |
Очень часто (особенно на фоне высоких доз гидрохлоро-тиазида) |
|
|
Гипомагниемия Гиперурикемия |
- |
- |
Часто |
|
|
Гиперкальциемия Гипергликемия Глюкозурия и ухудшение течения сахарного диабета |
- |
- |
Редко |
|
|
Гипохлоремический алкалоз |
- |
- |
Очень редко |
|
|
Нарушения психики |
Нарушение сна Депрессия |
- |
- |
Редко |
|
Нарушения со стороны нервной системы |
Головная боль |
Часто |
- |
Редко |
|
Парестезия |
Нечасто |
- |
Редко |
|
|
Головокружение |
Очень редко |
- |
Редко |
|
|
Обморок |
Частота неизвестна |
- |
- |
|
|
Нарушения со стороны органа зрения |
Нечеткость зрительного восприятия |
Нечасто |
- |
- |
|
Нарушение зрения (особенно в первые несколько недель лечения) |
- |
- |
Редко |
|
|
Острый приступ закрытоугольной глаукомы Хориоидальный выпот |
- |
- |
Частота неизвестна |
|
|
Нарушения со стороны органа слуха и лабиринтные нарушения |
Шум в ушах |
Нечасто |
- |
- |
|
Вертиго |
- |
Нечасто |
- |
|
|
Нарушения со стороны сердца |
Аритмии |
- |
- |
Редко |
|
Нарушения со стороны сосудов |
Выраженное снижение АД |
Нечасто |
- |
- |
|
Ортостатическая гипотензия (может усиливаться при одновременном применении этанола, седативных или обезболивающих средств) |
- |
- |
Часто |
|
|
Васкулит |
- |
Частота неизвестна |
- |
|
|
Периферические отеки |
Нечасто |
- |
- |
|
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Кашель |
Нечасто |
- |
- |
|
Некардиогенный отек легких |
Частота неизвестна |
- |
- |
|
|
Респираторный дистресс-синдром, включая отек легких и пневмонит |
- |
- |
Очень редко |
|
|
Нарушения со стороны желудочно-кишечного тракта |
Тошнота |
Нечасто |
- |
- |
|
Боль в животе |
- |
Нечасто |
- |
|
|
Диарея |
Очень редко |
- |
Редко |
|
|
Снижение аппетита Умеренно выраженные тошнота и рвота |
- |
- |
Часто |
|
|
Дискомфорт в животе Запор |
- |
- |
Редко |
|
|
Панкреатит |
- |
- |
Очень редко |
|
|
Нарушения со стороны печени и желчевыводя-щих путей |
Повышение активности «печеночных» ферментов в плазме крови |
- |
Частота неизвестна |
- |
|
Внутрипеченочный холестаз или желтуха |
- |
- |
Редко |
|
|
Нарушения со стороны кожи и подкожных тканей |
Ангионевротический отек Кожная сыпь Кожный зуд Буллезный дерматит |
- |
Частота неизвестна |
- |
|
Крапивница и другие формы кожной сыпи |
- |
- |
Часто |
|
|
Фотосенсибилизация |
- |
- |
Редко |
|
|
Некротизирующий васкулит и токсический эпидермальный некролиз Волчаночноподобные реакции Обострение кожных проявлений СКВ |
- |
- |
Очень редко |
|
|
Мультиформная эритема |
- |
- |
Частота неизвестна |
|
|
Нарушения со стороны скелетно-мышечной и соединительной ткани |
Миалгия |
Нечасто |
- |
- |
|
Мышечный спазм |
- |
- |
Частота неизвестна |
|
|
Артралгия |
Очень редко |
- |
- |
|
|
Нарушения со стороны почек и мочевыводящих путей |
Нарушение функции почек |
Частота неизвестна |
- |
Частота неизвестна |
|
Почечная недостаточность |
- |
Частота неизвестна |
- |
|
|
Острая почечная недостаточность (ОПН) |
- |
- |
Частота неизвестна |
|
|
Нарушения со стороны половых органов и молочной железы |
Импотенция |
- |
- |
Часто |
|
Общие расстройства и нарушения в месте введения |
Повышенная утомляемость |
Нечасто |
- |
- |
|
Гипертермия Астения |
- |
- |
Частота неизвестна |
|
|
Лабораторные и инструменталь-ные данные |
Повышение концентрации мочевой кислоты в сыворотке крови Повышение концентрации билирубина в сыворотке крови Повышение концентрации креатинина в сыворотке крови Гипонатриемия Гипокалиемия Нейтропения Повышение концентрации остаточного азота мочевины в сыворотке крови |
Частота неизвестна |
- |
- |
Сообщения об отдельных НР
Валсартан
Следующие НР наблюдались при изучении клинического применения валсартана у пациентов с артериальной гипертензией независимо от их причинной связи с применением валсартана: артралгия, астения, боль в спине, диарея, головокружение, головная боль, бессонница, снижение либидо, тошнота, отеки, фарингит, ринит, синусит, инфекции верхних дыхательных путей, вирусные инфекции.
Валсартан + гидрохлоротиазид
При изучении клинического применения фиксированной комбинации валсартан + гидрохлоротиазид у пациентов с артериальной гипертензией наблюдались следующие НР без очевидной связи с приемом препарата: боль в животе, боль в верхней части живота, тревога, артрит, астения, боль в спине, бронхит (в том числе острый), боль в груди, постуральное головокружение, диспепсия, одышка, сухость слизистой оболочки полости рта, носовое кровотечение, эректильная дисфункция, гастроэнтерит, головная боль, повышенное потоотделение, гипестезия, гриппоподобное состояние, бессонница, растяжение связок, мышечный спазм, мышечный гипертонус, заложенность носа, назофарингит, тошнота, боль в шее, периферические отеки, средний отит, боль в конечностях, учащенное сердцебиение, боль в гортани и глотке, пирексия, поллакиурия, гипертермия, синусит, сонливость, инфекции верхних дыхательных путей, инфекции мочевыводящих путей, вертиго, вирусные инфекции, нарушение зрения.
Ниже приведены НР, связанные с применением каждого компонента в отдельности.
Применение при беременности и кормлении грудью
Беременность
Валсартан
Применение АРА II в I триместре беременности не рекомендуется. Применение АРА II противопоказано во II-III триместрах беременности, поскольку применение во II-III триместрах беременности может вызывать фетотоксические эффекты (снижение функции почек, маловодие, замедление окостенения костей черепа плода) и неонатальные токсические эффекты (почечную недостаточность, артериальную гипотензию, гиперкалиемию). Имеются сообщения о самопроизвольных абортах у женщин, маловодии, а также о нарушении функции почек у новорожденных, матери которых во время беременности неумышленно получали валсартан.
Если препарат все-таки применялся во II-III триместрах беременности, то необходимо провести ультразвуковое исследование почек и костей черепа плода.
При планировании беременности рекомендуется пациентку перевести на альтернативную гипотензивную терапию с учетом профиля безопасности.
Новорожденные, матери которых получали АРА II во время беременности, нуждаются в медицинском наблюдении, так как существует риск развития артериальной гипотензии.
Гидрохлоротиазид
Опыт применения гидрохлоротиазида во время беременности, особенно в I триместре, ограничен. Гидрохлоротиазид проникает через плаценту. При применении тиазидных диуретиков во II-III триместре беременности возможно развитие тромбоцитопении, нарушения водно-электролитного баланса, желтухи у плода или новорожденного.
При подтверждении беременности препарат Вальсакор® НД 160 необходимо отменить как можно раньше.
Период грудного вскармливания
Нет данных о выделении валсартана в грудное молоко. Гидрохлоротиазид выделяется с грудным молоком у женщин.
При необходимости применения препарата Вальсакор® НД 160 в период лактации необходимо прекратить грудное вскармливание.
Противопоказания
- Гиперчувствительность к валсартану, гидрохлоротиазиду и к другим производным сульфонамида или любым другим компонентам препарата.
- Нарушения функции печени тяжелой степени (более 9 баллов по шкале Чайлд-Пью), билиарный цирроз и холестаз.
- Анурия.
- Нарушения функции почек тяжелой степени (КК менее 30 мл/мин).
- Рефрактерные гипокалиемия, гипонатриемия, гиперкальциемия и симптоматическая гиперурикемия.
- Одновременное применение с алискиреном и препаратами, содержащими алискирен, у пациентов с сахарным диабетом и/или с умеренными или тяжелыми нарушениями функции почек (скорость клубочковой фильтрации (СКФ) менее 60 мл/мин/1,73 м2 площади поверхности тела).
- Одновременное применение с ингибиторами АПФ у пациентов с диабетической нефропатией.
- Беременность и планирование беременности, период грудного вскармливания.
- Возраст до 18 лет (эффективность и безопасность применения у детей не доказаны).
- Дефицит лактазы, непереносимость лактозы, синдром глюкозо-галактозной мальабсорбции, так как в состав препарата Вальсакор® НД 160 входит лактоза.
Влияние на управление транспортными средствами и механизмами
В связи с возможностью возникновения головокружения или слабости на фоне применения препарата Вальсакор® НД 160 необходимо соблюдать осторожность при управлении транспортными средствами и механизмами, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Производитель и принимающий претензии
Наименование юридического лица, на имя которого выдано регистрационное удостоверение, адрес
АО «КРКА, д.д., Ново место», Шмарьешка цеста 6, 8501 Ново место, Словения
Производитель
АО «КРКА, д.д., Ново место», Шмарьешка цеста 6, 8501 Ново место, Словения
ООО «КРКА-РУС»,143500, Россия, Московская обл., г. Истра, ул. Московская, д. 50
Тел.: (495) 994-70-70, факс: (495) 994-70-78
Наименование и адрес организации, принимающей претензии потребителей
ООО «КРКА-РУС», 125212, г. Москва, Головинское шоссе, дом 5, корпус 1
Тел.: (495) 981-10-95, факс: (495) 981-10-91
Особые указания
Двойная блокада РААС
Одновременное применение АРА II, включая валсартан, с препаратами, содержащими алискирен, противопоказано у пациентов с сахарным диабетом и/или с умеренными или тяжелыми нарушениями функции почек (СКФ менее 60 мл/мин/1,73 м2 площади поверхности тела) и не рекомендуется у других пациентов.
Одновременное применение АРА II с ингибиторами АПФ противопоказано у пациентов с диабетической нефропатией и не рекомендуется у других пациентов.
Нарушение функции почек
У пациентов с нарушением функции почек (КК более 30 мл/мин) не требуется изменения дозы препарата. При применении препарата Вальсакор® НД 160 у пациентов с нарушением функции почек рекомендуется регулярно контролировать содержание калия, концентрации креатинина и мочевой кислоты в плазме крови.
Состояние после перенесенной трансплантации почки
Безопасность препарата Вальсакор® НД 160 у пациентов, недавно перенесших трансплантацию почки, не установлена.
Стеноз аортального и/или митрального клапанов, ГОКМП
Препарат Вальсакор® НД 160 необходимо с осторожностью применять у пациентов с гемодинамически значимым стенозом аортального и/или митрального клапанов или с ГОКМП.
Нарушение функции печени
Препарат Вальсакор® НД 160 не рекомендуется пациентам с нарушением функции печени. Максимально рекомендованная суточная доза валсартана у пациентов с нарушениями функции печени легкой или средней степения тяжести без явлений холестаза – 80 мг.
Нарушения водно-электролитного баланса
При применении тиазидных диуретиков, включая гидрохлоротиазид, отмечались случаи развития гипокалиемии, гипонатриемии и гипохлоремического алкалоза, гипомагниемии (так как увеличивается выведение магния почками) и гиперкальциемии (так как снижается выведение кальция почками). Рекомендуется при применении препарата Вальсакор® НД 160 регулярно контролировать содержание электролитов (особенно калия) в сыворотке крови.
Гипонатриемия и/или снижение ОЦК
У пациентов с выраженной гипонатриемией и/или при сниженном ОЦК (например, при приеме высоких доз диуретиков) в редких случаях в начале терапии препаратом Вальсакор® НД 160 возможно выраженное снижение уровня АД с клиническими проявлениями. Поэтому в начале лечения следует провести коррекцию содержания натрия в сыворотке крови и/или восполнить ОЦК.
В случае развития выраженного снижения АД пациента следует перевести в горизонтальное положение с приподнятыми ногами, и при необходимости провести в/в инфузию 0,9 % раствора натрия хлорида. После стабилизации уровня АД лечение препаратом Вальсакор® НД 160 может быть продолжено.
ХСН тяжелой степени (III-IV функционального класса по классификации NYHA) или другие заболевания, сопровождающиеся стимуляцией РААС
У пациентов, функция почек которых зависит от состояния РААС (например, ХСН III-IV функционального класса по классификации NYHA), терапия ингибиторами АПФ может сопровождаться олигурией и/или прогрессирующей азотемией, в редких случаях – ОПН. Невозможно исключить развитие нарушений функции почек вследствие подавления активности РААС на фоне приема препарата Вальсакор® НД 160. Терапию препаратом Вальсакор® НД 160 следует проводить с осторожностью, под контролем функции почек.
Первичный гиперальдостеронизм
Препарат Вальсакор® НД 160 не эффективен для лечения артериальной гипертензии у пациентов с первичным гиперальдостеронизмом по причине отсутствия активации РААС.
Стеноз почечной артерии
У пациентов с односторонним или двусторонним стенозом почечной артерии или стенозом артерии единственной почки препарат должен применяться с осторожностью, так как возможно повышение концентраций креатинина и мочевины в плазме крови.
Системная красная волчанка
При применении тиазидных диуретиков (в том числе гидрохлоротиазид) описаны случаи развития обострения и ухудшения течения заболеваний соединительной ткани (например, СКВ).
Фоточувствительность
Описаны случаи развития фоточувствительности на фоне приема гидрохлоротиазида. В случае развития проявлений фоточувствительности рекомендовано прекратить терапию. При необходимости продолжения терапии рекомендуется защищать открытые участки тела от воздействия солнечных и ультрафиолетовых (УФ) лучей.
НМРК
В двух фармакоэпидемиологических исследованиях, выполненных с использованием данных Датского национального регистра рака, была продемонстрирована связь между приемом гидрохлоротиазида и повышенным риском развития НМРК – базальноклеточной карциномы и плоскоклеточной карциномы. Риск развития НМРК возрастал при увеличении суммарной (накопленной) дозы гидрохлоротиазида. Возможным механизмом развития НМРК является фотосенсибилизирующее действие гидрохлоротиазида.
Пациенты, принимающие гидрохлоротиазид в качестве монотерапии или в комбинации с другими лекарственными препаратами, должны быть осведомлены о риске развития НМРК. Таким пациентам рекомендуется регулярно осматривать кожные покровы с целью выявления любых новых подозрительных поражений, а также изменений уже имеющихся поражений кожи.
Обо всех подозрительных изменениях кожи следует незамедлительно сообщать врачу. Подозрительные участки кожи должны быть обследованы специалистом. Для уточнения диагноза может потребоваться гистологическое исследование биоптатов кожи.
С целью минимизации риска развития НМРК пациентам следует рекомендовать соблюдать профилактические меры, такие как ограничение воздействия солнечного света и УФ лучей, а также использование соответствующих защитных средств.
У пациентов с НМРК в анамнезе рекомендуется пересмотреть целесообразность применения гидрохлоротиазида.
Другие метаболические нарушения
Тиазидные диуретики, включая гидрохлоротиазид, могут вызывать изменение толерантности к глюкозе и повышение концентрации холестерина, триглицеридов и мочевой кислоты в плазме крови.
Пациентам с сахарным диабетом может потребоваться коррекция дозы инсулина или гипогликемических средств для приема внутрь.
Тиазидные диуретики снижают экскрецию ионов кальция почками и могут вызывать незначительное повышение содержания кальция в плазме крови при отсутствии сопутствующих нарушений метаболизма кальция. Выраженная гиперкальциемия на фоне применения тиазидного диуретика может свидетельствовать о гиперпаратиреозе. Перед исследованием функции паращитовидных желез следует отменить тиазидные диуретики, включая гидрохлоротиазид.
Антидопинговый тест
Гидрохлоротиазид может давать положительный результат при проведении допинг-контроля.
Реакции гиперчувствительности
Реакции гиперчувствительности на фоне применения гидрохлоротиазида наиболее часто отмечались у пациентов с аллергическими реакциями и бронхиальной астмой в анамнезе.
При применении валсартана у пациентов наблюдалось развитие ангионевротического отека, в том числе отека гортани и голосовых связок, приводящего к обструкции дыхательных путей, и/или отека лица, губ, глотки и/или языка. У некоторых из этих пациентов в анамнезе отмечалось развитие ангионевротического отека на фоне применения других лекарственных средств, включая ингибиторы АПФ. В случае развития ангионевротического отека следует немедленно отменить препарат Вальсакор® НД 160 и в дальнейшем не возобновлять лечение препаратом.
Хориоидальный выпот/острая миопия/острая вторичная закрытоугольная глаукома
Сульфонамиды и их производные могут вызывать идиосинкразическую реакцию, приводящую к развитию хориоидального выпота с нарушением полей зрения, острой миопии и острому приступу вторичной закрытоугольной глаукомы. Симптомы включают в себя внезапное снижение остроты зрения или боль в глазу; возникают, как правило, в течение нескольких часов или недель после начала терапии тиазидным/тиазидоподобным диуретиком. При отсутствии лечения острая вторичная закрытоугольная глаукома может привести к необратимой потере зрения. При появлении симптомов необходимо как можно быстрее прекратить прием тиазидного/тиазидоподобного диуретика. Если внутриглазное давление остается неконтролируемым, может потребоваться неотложное медикаментозное лечение или хирургическое вмешательство. Фактором риска развития острой закрытоугольной глаукомы является аллергическая реакция на производные сульфонамида и/или пенициллины в анамнезе.
Специальная информация о вспомогательных веществах
Препарат Вальсакор® НД 160 содержит лактозу, поэтому противопоказан пациентам с непереносимостью лактозы, дефицитом лактазы, синдромом глюкозо-галактозной мальабсорбции.
Меры предосторожности
С осторожностью
Одновременное применение калийсберегающих диуретиков, препаратов калия, калийсодержащих пищевых добавок или других лекарственных препаратов, способных повышать содержание калия в сыворотке крови (например, гепарин). Одновременное применение с лекарственными препаратами, которые могут вызывать полиморфную желудочковую тахикардию типа «пируэт» или увеличивать продолжительность интервала QT на электрокардиограмме (ЭКГ), а также применение c лекарственными препаратами, способными вызывать гипокалиемию, и сердечными гликозидами.
Хроническая сердечная недостаточность (ХСН) III-IV функционального класса по классификации NYHA, стеноз аортального и/или митрального клапана, гипертрофическая обструктивная кардиомиопатия (ГОКМП), увеличение длительности интервала QT на ЭКГ.
Умеренно выраженные нарушения функции печени без явлений холестаза, обструктивные заболевания желчевыводящих путей.
Cостояния, сопровождающиеся водно-электролитными нарушениями: нефропатия с потерей солей и преренальным (кардиогенным) нарушением функции почек, гипокалиемия, гипонатриемия, гипомагниемия, гиперкальциемия. Двусторонний или односторонний стеноз почечных артерий или стеноз артерии единственной почки, состояние после трансплантации почки, выраженная гипонатриемия и/или состояния, сопровождающиеся снижением ОЦК (в том числе диарея, рвота, терапия высокими дозами диуретиков).
Первичный гиперальдостеронизм, гиперпаратиреоз, гиперурикемия, сахарный диабет, гиперхолестеринемия, гипертриглицеридемия, системная красная волчанка (СКВ), немеланомный рак кожи (НМРК) в анамнезе (см. раздел «Особые указания»).
У пациентов с аллергической реакцией на пенициллин в анамнезе, с наследственным ангионевротическим отеком, либо ангионевротическим отеком на фоне предшествующей терапии АРА II или ингибиторами АПФ.
Условия хранения
При температуре не выше 25 °С, в оригинальной упаковке.
Хранить в недоступном для детей месте.
Лекарственная форма
таблетки, покрытые пленочной оболочкой
Способ применения и дозы
Перед началом терапии препаратом Вальсакор® НД 160 необходимо скорректировать водно-электролитные нарушения (см. разделы «С осторожностью», «Особые указания»).
Внутрь, один раз в сутки, ежедневно, независимо от времени приема пищи. Таблетку следует проглатывать целиком и запивать достаточным количеством жидкости.
Рекомендуемая суточная доза – 1 таблетка препарата Вальсакор® НД 160.
Доза препарата Вальсакор® НД 160 подбирается после ранее проведенного титрования доз отдельных компонентов препарата. При недостаточности антигипертензивного эффекта возможно увеличение дозы препарата (не ранее, чем через 4-6 недель) путем титрования доз до максимальной суточной дозы в пересчете на валсартан 320 мг и до максимальной суточной дозы по гидрохлоротиазиду 25 мг.
Максимальное снижение уровня АД обычно достигается в течение 2-4 недель терапии, но у некоторых пациентов – в течение 4-8 недель, что необходимо учитывать при титровании дозы.
Пациенты с нарушением функции почек
Пациентам с нарушением функции почек легкой или средней степени тяжести (КК ≥ 30 мл/мин (0,5 мл/сек)) коррекции дозы препарата Вальсакор® НД 160 не требуется.
Пациенты с нарушением функции печени
Максимально рекомендованная суточная доза валсартана у пациентов с нарушением функции печени легкой (5-6 баллов по шкале Чайлд-Пью) или средней (7-9 баллов по шкале Чайлд-Пью) степени тяжести без явлений холестаза составляет 80 мг.
Фармакологические свойства
Препарат Вальсакор® НД 160 – комбинированный гипотензивный препарат, в состав которого входят антагонист рецепторов ангиотензина II (АРА II) и тиазидный диуретик.
Фармакодинамика
Валсартан
Валсартан является селективным АРА II для приема внутрь небелковой природы.
Избирательно блокирует АТ1-рецепторы, ответственные за вазопрессорное действие ангиотензина II. Следствием блокады АТ1-рецепторов является повышение концентрации ангиотензина II в плазме крови, которое может стимулировать незаблокированные АТ2-рецепторы, что уравновешивает вазопрессорные эффекты, связанные с возбуждением АТ1-рецепторов. Валсартан не имеет агонистической активности в отношении АТ1-рецепторов. Его сродство к АТ1-рецепторам примерно в 20000 раз выше, чем к АТ2-рецепторам.
Валсартан не ингибирует ангиотензинпревращающий фермент (АПФ), известный также как кининаза II, который превращает ангиотензин I в ангиотензин II и разрушает брадикинин. В связи с отсутствием влияния на АПФ, не потенцируются эффекты брадикинина и субстанции Р. Частота развития сухого кашля ниже у пациентов, получавших АРА II, в сравнении с пациентами, получавшими ингибиторы АПФ. Валсартан не вступает во взаимодействие и не блокирует рецепторы других гормонов или ионные каналы, участвующие в регуляции функций сердечно-сосудистой системы.
При лечении артериальной гипертензии валсартан снижает артериальное давление (АД), не влияя на частоту сердечных сокращений (ЧСС).
После приема внутрь разовой дозы валсартана антигипертензивный эффект развивается в течение 2 часов, а максимальное снижение АД достигается через 4-6 часов. Антигипертензивный эффект валсартана сохраняется в течение 24 часов после его применения. При постоянном применении валсартана максимальное снижение АД вне зависимости от дозы достигается через 2-4 недели и поддерживается на достигнутом уровне в ходе длительной терапии.
Одновременное применение с гидрохлоротиазидом позволяет достичь значимого дополнительного снижения АД.
Внезапная отмена валсартана не сопровождается резким повышением АД или другими нежелательными клиническими последствиями.
Гидрохлоротиазид
Точкой приложения действия тиазидных диуретиков являются дистальные извитые почечные канальцы. При воздействии тиазидных диуретиков на высокочувствительные рецепторы дистальных канальцев коркового слоя почек происходит подавление реабсорбции ионов натрия (Na+) и хлора (Cl-). Подавление ко-транспортной системы Na+ и Cl-, по-видимому, происходит за счет конкуренции за участки связывания Cl- в данной системе, что приводит к увеличению экскреции ионов Na+ и Cl- примерно в одинаковой степени.
В результате диуретического действия наблюдается уменьшение объема циркулирующей крови (ОЦК), вследствие чего повышается активность ренина, секреция альдостерона, выведение почками калия и, следовательно, снижение содержания калия в сыворотке крови. Связь между ренином и альдостероном опосредуется ангиотензином II, поэтому снижение содержания калия в сыворотке крови при одновременном применении гидрохлоротиазида с валсартаном менее выражено, чем при монотерапии гидрохлоротиазидом.
Фармакокинетика
Валсартан
Всасывание
После приема валсартана внутрь максимальная концентрация (Cmax) в плазме крови достигается в течение 2-4 часов. Средняя абсолютная биодоступность составляет 23 %. При приеме валсартана с пищей площадь под кривой «концентрация-время» (AUC) и Cmax в плазме крови уменьшаются на 40 % и 50 % соответственно. Тем не менее, через 8 часов после приема валсартана, принятого натощак и с пищей, его плазменные концентрации были одинаковы в обеих группах. Уменьшение AUC не сопровождается клинически значимым снижением терапевтического эффекта валсартана, поэтому валсартан можно принимать независимо от времени приема пищи.
Распределение
Объем распределения (Vd) валсартана в период равновесного состояния после внутривенного (в/в) введения составлял около 17 л, что указывает на отсутствие выраженного распределения валсартана в тканях. Валсартан активно связывается с белками плазмы крови (94-97 %), преимущественно с альбумином.
Метаболизм
Валсартан не подвергается существенной биотрансформации, только около 20 % дозы, принятой внутрь, выводится в виде метаболитов. Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее 10 % от AUC валсартана). Этот метаболит не обладает фармакологической активностью.
Выведение
Валсартан выводится двухфазно: a-фаза с периодом полувыведения (Т½a) менее 1 часа и b-фаза с Т½b – около 9 часов. Валсартан выводится в основном в неизмененном виде через кишечник (около 83 %) и почками (около 13 %). После в/в введения плазменный клиренс валсартана составляет около 2 л/час, почечный клиренс – 0,62 л/час (около 30 % от общего клиренса). Т½ валсартана составляет 6 часов.
Фармакокинетика валсартана в диапазоне терапевтических доз носит линейный характер. При повторном применении валсартана изменений фармакокинетических показателей не отмечалось. При приеме валсартана один раз в сутки кумуляция незначительна. Плазменные концентрации валсартана одинаковы у мужчин и женщин.
Гидрохлоротиазид
Всасывание
При приеме внутрь гидрохлоротиазид всасывается быстро. Cmax в плазме крови достигается через 2 часа после приема внутрь. В терапевтическом диапазоне доз средняя величина AUC возрастает прямо пропорционально относительно увеличению дозы. Одновременный прием с пищей может привести к увеличению или уменьшению системной доступности по сравнению с приемом натощак, данные изменения не имеют клинического значения. При приеме внутрь абсолютная биодоступность гидрохлоротиазида составляет 70 %.
Распределение
Видимый Vd составляет 4-8 л/кг. Связывание с белками плазмы крови (преимущественно с альбуминами) составляет около 40-70 %. Гидрохлоротиазид накапливается в эритроцитах в концентрации, примерно в три раза превышающей плазменную.
Метаболизм, выведение
Гидрохлоротиазид элиминируется практически в неизмененном виде. Т½ конечной фазы составляет 6-15 часов. При повторном применении фармакокинетика гидрохлоротиазида не изменяется. При приеме один раз в сутки накопление гидрохлоротиазида незначительно. Более 95 % абсорбировавшейся дозы выводится в неизмененном виде почками.
Валсартан + гидрохлоротиазид
При одновременном применении с валсартаном системная биодоступность гидрохлоротиазида уменьшается на 30 %, а биодоступность валсартана существенно не изменяется.
Отмеченное взаимодействие не оказывает влияние на эффективность комбинированного применения валсартана и гидрохлоротиазида. В контролируемых клинических исследованиях был выявлен отчетливый антигипертензивный эффект данной комбинации, который превышал эффект каждого из действующих веществ препарата в отдельности или эффект плацебо.
Фармакокинетика у особых групп пациентов
Пациенты пожилого возраста (старше 65 лет)
AUC валсартана у некоторых пациентов пожилого возраста больше, чем у добровольцев молодого возраста. Данные изменения клинического значения не имеют.
Предположительно, у пациентов пожилого возраста с нормальным уровнем АД и артериальной гипертензией системный клиренс гидрохлоротиазида ниже, чем у здоровых молодых добровольцев.
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек с клиренсом креатинина (КК) 30-70 мл/мин коррекции дозы препарата Вальсакор® НД 160 не требуется. Нет данных по применению препарата у пациентов с нарушением функции почек тяжелой степени (КК менее 30 мл/мин) и у пациентов, находящихся на гемодиализе. Валсартан не выводится с помощью гемодиализа, в отличие от гидрохлоротиазида.
При наличии почечной недостаточности Cmax и AUC гидрохлоротиазида увеличиваются, а скорость выведения снижается. У пациентов с нарушением функции почек легкой и средней степени тяжести T½ гидрохлоротиазида удлиняется практически в два раза.
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени легкой (5-6 баллов по шкале Чайлд-Пью) или средней (7-9 баллов по шкале Чайлд-Пью) степени тяжести AUC валсартана в два раза больше, чем у здоровых добровольцев. Нет данных по применению валсартана у пациентов с нарушением функции печени тяжелой степени (более 9 баллов по шкале Чайлд-Пью).
Заболевания печени не оказывают существенного влияния на фармакокинетику гидрохлоротиазида, поэтому коррекции его дозы в данном случае не требуется.
У пациентов с обструкцией желчевыводящих путей препарат Вальсакор® НД 160 следует применять с осторожностью.
Взаимодействие с другими лекарственными препаратами и другие виды взаимодействия
Валсартан + гидрохлоротиазид
Не рекомендуется
Препараты лития
При одновременном применении ингибиторов АПФ, АРА II или тиазидных диуретиков с препаратами лития отмечалось обратимое повышение концентрации лития в плазме крови и развитие интоксикации. Риск токсических проявлений, связанных с применением препаратов лития, может дополнительно увеличиваться при одновременном применении с препаратом Вальсакор® НД 160, поскольку почечный клиренс препаратов лития снижается под действием тиазидных диуретиков. При необходимости одновременного применения с препаратами лития следует тщательно контролировать концентрацию лития в плазме крови.
С осторожностью
Другие гипотензивные препараты
Возможно усиление антигипертензивного эффекта при одновременном применении с другими лекарственными средствами, снижающими АД (например, ингибиторы АПФ, бета-адреноблокаторы, блокаторы «медленных» кальциевых каналов, гуанетидин, метилдопа, вазодилататоры, прямые ингибиторы ренина, АРА II).
Прессорные амины (например, норэпинефрин и эпинефрин)
Возможно ослабление действия прессорных аминов, не требующее прекращения одновременного применения валсартана и гидрохлоротиазида.
Нестероидные противовоспалительные препараты (НПВП), включая селективные ингибиторы циклооксигеназы-2 (ЦОГ-2)
При одновременном применении АРА II и гидрохлоротиазида с НПВП возможно ослабление диуретического и антигипертензивного действия. В условиях гиповолемии возможно развитие ОПН; рекомендуется контролировать функцию почек в начале терапии, а также проводить адекватное восполнение ОЦК у пациента.
Валсартан
Противопоказано
Двойная блокада ренин-ангиотензин-альдостероновой системы (РААС)
Одновременное применение АРА II, включая валсартан, с препаратами, содержащими алискирен, противопоказано у пациентов с сахарным диабетом и/или с умеренными или тяжелыми нарушениями функции почек (СКФ менее 60 мл/мин/1,73 м2 площади поверхности тела) и не рекомендуется у других пациентов.
Одновременное применение АРА II с ингибиторами АПФ противопоказано у пациентов с диабетической нефропатией и не рекомендуется у других пациентов.
Не рекомендуется
Калийсберегающие диуретики (спиронолактон, эплеренон, триамтерен, амилорид), препараты калия, калийсодержащие заменители пищевой соли и другие лекарственные средства и вещества, которые могут вызывать повышение содержания калия в сыворотке крови (например, гепарин)
При необходимости одновременного применения с препаратами, влияющими на содержание калия, рекомендуется контролировать содержание калия в плазме крови.
С осторожностью
При одновременном применении АРА II, включая валсартан, с лекарственными средствами, оказывающими влияние на РААС, такими как ингибиторы АПФ или алискирен, повышается частота возникновения случаев артериальной гипотензии, гиперкалиемии, нарушения функции почек. Необходимо контролировать АД, функцию почек, содержание электролитов в плазме крови у таких пациентов.
Белки-переносчики
Исследования in vitro на культурах печени показали, что валсартан является субстратом для белков-переносчиков OATP1B1/OATP1B3 и MRP2. Одновременное применение валсартана с ингибиторами белка-переносчика OATP1B1/OATP1B3 (рифампицин, циклоспорин) или MRP2 (ритонавир) может увеличивать системную экспозицию валсартана (Cmax и AUC). Необходимо соблюдать осторожность в начале одновременного применения с вышеуказанными препаратами или после их отмены.
Отсутствие лекарственного взаимодействия
Не выявлено клинически значимых взаимодействий со следующими лекарственными средствами: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, гидрохлоротиазид, амлодипин и глибенкламид.
Гидрохлоротиазид
Не рекомендуется
Препараты лития
При одновременном применении гидрохлоротиазида и препаратов лития снижается почечный клиренс лития, что может привести к повышению концентрации лития в плазме крови и увеличению его токсичности. При необходимости одновременного применения гидрохлоротиазида следует тщательно подбирать дозу препаратов лития, регулярно контролировать концентрацию лития в плазме крови и соответствующим образом подбирать дозу препарата.
Требуется особое внимание
Препараты, способные вызывать полиморфную желудочковую тахикардию типа «пируэт»
Следует с особой осторожностью применять гидрохлоротиазид одновременно с такими препаратами, как:
- антиаритмические лекарственные препараты I А класса (хинидин, гидрохинидин, дизопирамид, прокаинамид) и I С класса (флекаинид);
- антиаритмические лекарственные препараты III класса (дофетилид, ибутилид, бретилия тозилат), соталол, дронедарон, амиодарон;
- другие (неантиаритмические) лекарственные средства, такие как:
- нейролептики: фенотиазины (хлорпромазин, циамемазин, левомепромазин, тиоридазин, трифлуоперазин, флуфеназин), бензамиды (амисульприд, сультоприд, сульприд, тиаприд), бутирофеноны (дроперидол, галоперидол), пимозид, сертиндол;
- антидепрессанты: трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина (циталопрам, эсциталопрам);
- антибактериальные средства: фторхинолоны (левофлоксацин, моксифлоксацин, спарфлоксацин, ципрофлоксацин), макролиды (эритромицин при в/в введении, азитромицин, кларитромицин, рокситромицин, спирамицин), ко-тримоксазол;
- противогрибковые средства: азолы (вориконазол, итраконазол, кетоконазол, флуконазол);
- противомалярийные средства (хинин, хлорохин, мефлохин, галофантрин, лумефантрин);
- противопротозойные средства (пентамидин при парентеральном введении);
- антиангинальные средства (ранолазин, бепридил);
- противоопухолевые средства (вандетаниб, мышьяка триоксид, оксалиплатин, такролимус);
- противорвотные средства (домперидон, ондансетрон);
- средства, влияющие на моторику желудочно-кишечного тракта (цизаприд);
- антигистаминные средства (астемизол, терфенадин; мизоластин);
- прочие лекарственные средства (анагрелид, вазопрессин, дифеманила метилсульфат, кетансерин, пробукол, пропофол, севофлуран, терлипрессин, теродилин, цилостазол).
В связи с увеличением риска желудочковых аритмий, особенно полиморфной желудочковой тахикардии типа «пируэт» (фактор риска – гипокалиемия) следует определять содержание калия в плазме крови и при необходимости корректировать его до начала комбинированной терапии гидрохлоротиазидом с указанными выше препаратами. Необходим контроль клинического состояния пациента, содержания электролитов плазмы крови и показателей ЭКГ. У пациентов с гипокалиемией необходимо применять препараты, не вызывающие полиморфную желудочковую тахикардию типа «пируэт».
Лекарственные средства, способные увеличивать продолжительность интервала QT
Одновременное применение гидрохлоротиазида с лекарственными препаратами, способными увеличивать продолжительность интервала QT, должно основываться на тщательной оценке для каждого пациента соотношения ожидаемой пользы и потенциального риска (возможно увеличение риска развития полиморфной желудочковой тахикардии типа «пируэт»). При применении таких комбинаций необходимо регулярно контролировать ЭКГ (для выявления удлинения интервала QT), а также контролировать содержание калия в плазме крови.
Препараты, способные вызывать гипокалиемию: амфотерицин В (при в/в введении), глюко- и минералокортикостероиды (при системном применении), тетракозактид, глицирризиновая кислота (карбеноксолон, препараты, содержащие корень солодки), слабительные средства, стимулирующие моторику кишечника
Увеличение риска развития гипокалиемии при одновременном применении с гидрохлоротиазидом (аддитивный эффект). Необходим регулярный контроль содержания калия в плазме крови, при необходимости – его коррекция. На фоне терапии гидрохлоротиазидом рекомендуется применять слабительные средства, не стимулирующие моторику кишечника.
Сердечные гликозиды
Гипокалиемия и гипомагниемия, обусловленные действием тиазидных диуретиков, усиливают токсичность сердечных гликозидов. При одновременном применении гидрохлоротиазида и сердечных гликозидов следует регулярно контролировать содержание калия в плазме крови, показатели ЭКГ, и при необходимости корректировать терапию.
Требуется внимание
Другие гипотензивные препараты
Потенцирование антигипертензивного действия гидрохлоротиазида (аддитивный эффект). Может появиться необходимость в коррекции дозы одновременно назначенных гипотензивных препаратов.
Рекомендуется прекратить прием гидрохлоротиазида за 2-3 дня до начала терапии ингибиторами АПФ для предотвращения развития симптоматической артериальной гипотензии. Если это невозможно, то следует снизить начальную дозу ингибиторов АПФ.
Этанол, барбитураты, антипсихотические средства (нейролептики), антидепрессанты, анксиолитики, наркотические анальгетики и средства для общей анестезии
Возможно усиление антигипертензивного действия гидрохлоротиазида и потенцирование ортостатической гипотензии (аддитивный эффект).
Недеполяризирующие миорелаксанты (например, тубокурарин)
Возможно усиление эффекта недеполяризирующих миорелаксантов.
Адреномиметики (прессорные амины)
Гидрохлоротиазид может снижать эффект адреномиметиков, таких как эпинефрин (адреналин) и норэпинефрин (норадреналин).
НПВП, включая ЦОГ-2 и высокие дозы ацетилсалициловой кислоты (≥ 3 г/сутки)
НПВП могут снижать диуретическое и антигипертензивное действия гидрохлоротиазида. При одновременном применении существует риск развития ОПН вследствие снижения СКФ. Гидрохлоротиазид может усиливать токсическое действие высоких доз салицилатов на центральную нервную систему.
Гипогликемические средства для приема внутрь и инсулин
Тиазидные диуретики влияют на толерантность к глюкозе (возможно развитие гипергликемии) и снижают эффективность гипогликемических средств (может потребоваться коррекция дозы гипогликемических средств).
Следует с осторожностью одновременно применять гидрохлоротиазид и метформин в связи с риском развития лактоацидоза на фоне нарушения функции почек, вызванного гидрохлоротиазидом.
Бета-адреноблокаторы, дuазоксид
Одновременное применение тиазидных диуретиков (включая гидрохлоротиазид) с бета-адреноблокаторами или диазоксидом может увеличивать риск развития гипергликемии.
Лекарственные препараты, применяющиеся для лечения подагры (пробенецид, сульфинпиразон, аллопуринол)
Может потребоваться коррекция дозы урикозурических лекарственных средств, так как гидрохлоротиазид увеличивает концентрацию мочевой кислоты в сыворотке крови. Тиазидные диуретики могут увеличивать частоту развития реакций гиперчувствительности к аллопуринолу.
Амантадин
Тиазидные диуретики (включая гидрохлоротиазид) могут снижать клиренс амантадина, приводить к повышению концентрации амантадина в плазме крови и увеличивать риск его НР.
Антихолинергические препараты (холиноблокаторы)
Антихолинергические препараты (например, атропин, бипериден) увеличивают биодоступность тиазидных диуретиков за счет снижения моторики желудочно-кишечного тракта и скорости опорожнения желудка.
Цитотоксические (противоопухолевые) препараты
Тиазидные диуретики уменьшают почечную экскрецию цитотоксических лекарственных средств (например, циклофосфамида и метотрексата) и потенцируют их миелосупрессивное действие.
Метuлдопа
Описаны случаи гемолитической анемии при одновременном применении гидрохлоротиазида и метилдопы.
Противоэпилептические препараты (карбамазепин, окскарбазепин, топирамат)
Риск развития симптоматической гипонатриемии. При одновременном применении гидрохлоротиазида и карбамазепина необходимо наблюдение за состоянием пациента и контроль содержания натрия в сыворотке крови. При одновременном применении гидрохлоротиазида и топирамата также следует контролировать концентрацию топирамата в сыворотке крови, при необходимости следует назначить препараты калия или корректировать дозу топирамата.
Селективные ингибиторы обратного захвата серотонина
При одновременном применении с тиазидными диуретиками возможно потенцирование гипонатриемии. Необходим контроль содержания натрия в плазме крови.
Циклоспорин
При одновременном применении тиазидных диуретиков и циклоспорина увеличивается риск развития гиперурикемии и обострения подагры.
Пероральные антикоагулянты
Тиазидные диуретики могут уменьшать эффект пероральных антикоагулянтов.
Йодсодержащие контрастные вещества
Обезвоживание организма на фоне приема тиазидных диуретиков увеличивает риск развития ОПН, особенно при применении высоких доз йодсодержащих контрастных веществ. Перед применением йодсодержащих контрастных веществ необходимо компенсировать потерю жидкости.
Препараты кальция
При одновременном применении возможно повышение содержания кальция в крови и развитие гиперкальциемии вследствие снижения выведения ионов кальция почками. Если необходимо одновременное назначение кальцийсодержащих лекарственных средств, то следует контролировать содержание кальция в плазме крови и корректировать дозу препаратов кальция.
Анионные обменные смолы (колестирамин и колестипол)
Анионные обменные смолы уменьшают абсорбцию гидрохлоротиазида. Однократные дозы колестирамина и колестипола уменьшают всасывание гидрохлоротиазида в желудочно-кишечном тракте на 85 % и 43 % соответственно.